Diferența principală: Atomii sunt unitățile de bază din care este făcută toată materia. Atomii sunt mici, variind între 0, 1 și 0, 5 nanometri în lățime. Fiecare atom din orice element este format din protoni, neutroni și electroni. Atomii unor elemente diferite se reunesc pentru a face molecule. Acest lucru se întâmplă printr-o reacție chimică. O moleculă este cea mai mică cantitate de substanță chimică care poate exista.
Un element este o substanță chimică pură care are unul sau un tip de atom, distingându-se prin numărul său atomic. Numărul atomic este derivat din numărul de protoni prezenți în nucleul elementului. Există un total de 118 elemente care au fost identificate, împărțite între metal, metaloide și nemetale. Fiecare element are propriul său set de proprietăți. Cele mai multe elemente sunt disponibile pe pământ, în timp ce câteva au fost dezvoltate artificial prin reacții nucleare. Un element este deja în cea mai crudă formă și nu poate fi defalcat în continuare. Toate elementele pot fi găsite în tabelul periodic, listate după numărul atomic.
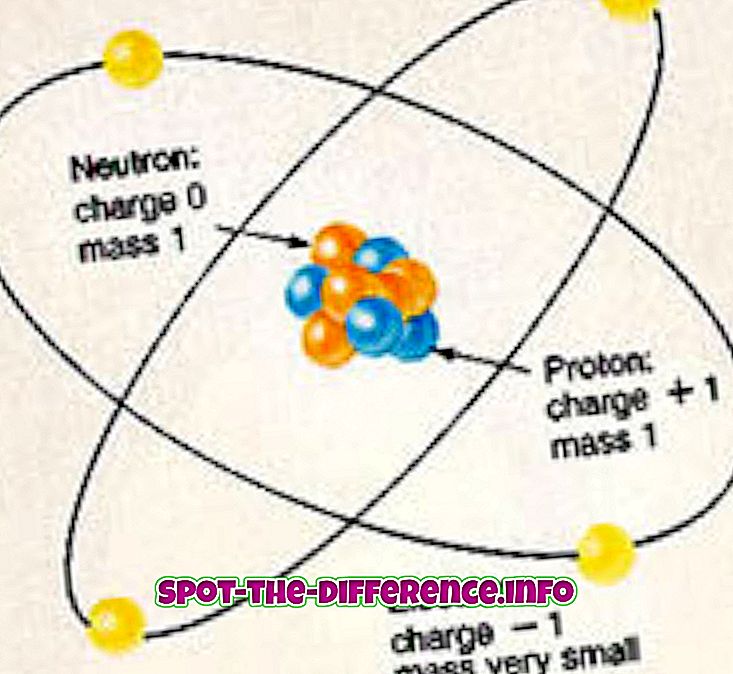
Fiecare atom din orice element este format din protoni, neutroni și electroni. Protonii și neutronii formează nucleul atomului și sunt situați în mijlocul atomului. Nucleul este înconjurat de un nor de electroni care sunt legați de nucleu printr-o forță electromagnetică. Electronii au o sarcină negativă care este modul în care sunt atrase de nucleu, deoarece protonii din nucleu au o încărcătură pozitivă. Neutronii, pe de altă parte, nu au nicio taxă.
Numărul de protoni, neutroni și electroni dintr-un atom determină ce element este. De exemplu: Un atom de fier are 26 de protoni, 30 de neutroni și 26 de electroni. Fiecare atom de fier va avea această configurație.
Atomii unor elemente diferite se reunesc pentru a face molecule. Acest lucru se întâmplă printr-o reacție chimică. De exemplu: doi atomi de hidrogen și un atom de oxigen se combină pentru a forma o moleculă de apă.

O moleculă poate avea proprietăți foarte diferite de elementele din care este fabricată. De exemplu: apa se comportă foarte diferit decât oxigenul sau hidrogenul, chiar dacă este compus din doi atomi de hidrogen și un atom de oxigen.
În plus, un atom nu poate exista independent în natură fără a se lega de ceva. Nu vom găsi niciodată doar un singur atom de oxigen sau un singur atom de carbon. Este întotdeauna legat de ceva, cum ar fi O2 (oxigen) sau CO2 (dioxid de carbon). Când este legat într-o moleculă, molecula poate exista independent în natură, de aceea găsim mereu o moleculă de oxigen, o moleculă de dioxid de carbon, o moleculă de apă (H2O) etc.
Într-o moleculă, atomii sunt blocați împreună într-o anumită formă sau formă. Acest lucru depinde în principal de numărul de obligațiuni pe care atomul le poate face. Atomii formează molecule prin formarea de legături chimice între ele. Atomii de oxigen au întotdeauna două legături cu alți atomi, atomii de carbon au întotdeauna patru legături cu alți atomi, iar atomii de azot au întotdeauna trei legături cu alți atomi. Prin urmare, un anumit tip de moleculă are întotdeauna o formă particulară, cum ar fi pentagonală, hexagonală, laterală, bi-laterală etc.
Moleculele tind să se unească întotdeauna, formarea lor depinzând de starea lor. Cum ar fi într-o stare gazoasă, moleculele tind să fie doar în zbor. Într-o stare lichidă, moleculele tind să fie grupate împreună, astfel încât să se poată mișca. Într-o stare solidă, moleculele sunt împachetate bine și pot vibra numai.
Moleculele sunt de obicei reprezentate într-o formulă moleculară. De exemplu: O2, H2O, CO2, C6H12O6 (zahăr). Formula moleculară este numele elementului urmat de numărul atomilor acelui element din moleculă.