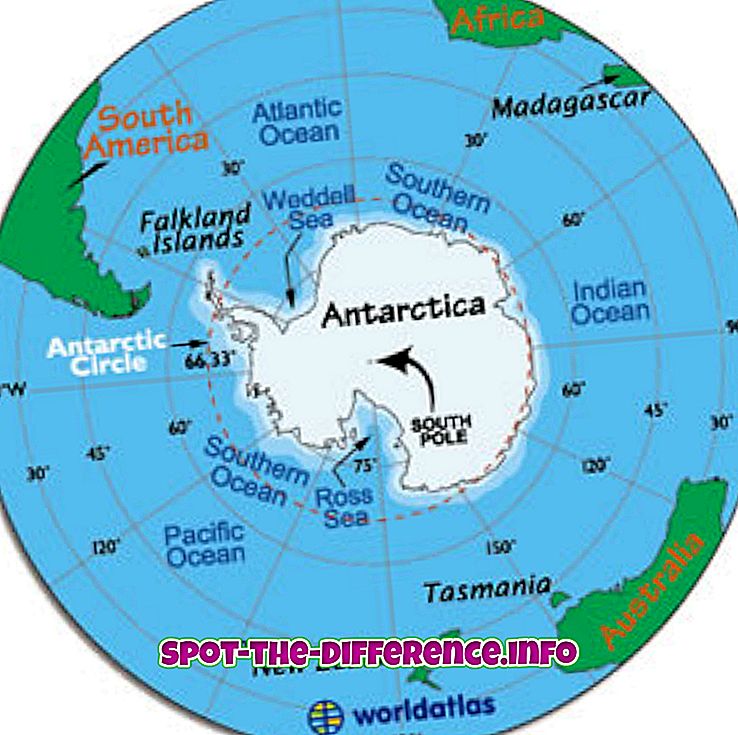
Diferența cheie: masa atomică este pur și simplu masa unui izotop specific, sau masa combinată a protonilor, a neutronilor și a electronilor atomului. Numărul atomic este numărul de protoni care se găsește într-un nucleu al unui element.
Să ne confruntăm cu chimia este confuză, cu diferitele elemente, numere atomice, legături, masă, greutate, atomi etc. Toate aceste cuvinte încep să se estompeze după o anumită perioadă de timp, încât o persoană nu mai poate distinge unul de celălalt. Ei bine, masa atomică și numărul atomic sunt două dintre astfel de cuvinte care sunt adesea confundate și folosite interschimbabil.
Masa atomică este masa unui atom când este în repaus. Acest lucru se datorează faptului că atunci când un atom se mișcă la o viteză foarte mare, acesta tinde să crească în masă. Deși, conform definiției, masa atomică este masa tuturor protonilor, a neutronilor și a electronilor, electronii sunt prea mici pentru a face orice diferență semnificativă în masa atomică. Majoritatea elementelor de pe masa periodică au izotopi și datorită diferenței în numărul de neutroni, masa fiecărui izotop se schimbă, de asemenea.
Masa atomică este exprimată utilizând unități de masă atomică sau amu. O unitate de masă atomică este egală cu 1/12 din masa carbonului-12. Atunci când masa unui atom este împărțită la 1/12 din masa Carbon-12, se obține masa relativă a elementului. Cu toate acestea, masa relativă a unui obiect este, de fapt, greutatea atomică a unui element, așa cum se calculează prin considerarea tuturor izotopilor. Deși, acest lucru nu ar trebui să fie considerat ca masa atomică a unui element.

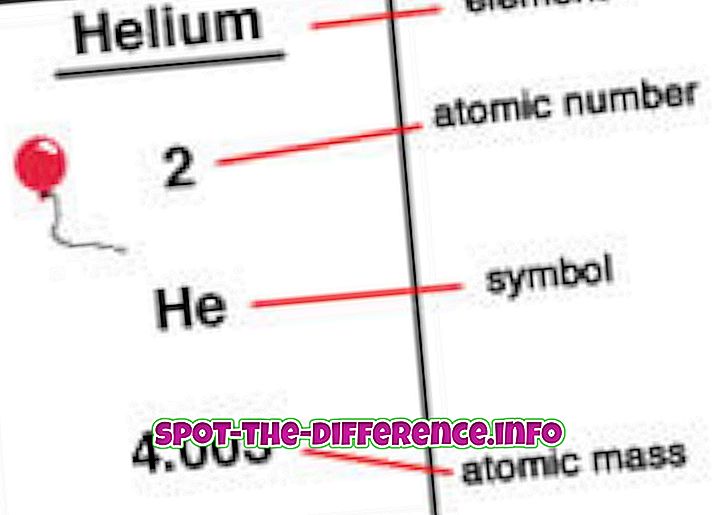
Numărul atomic este numărul de protoni care se găsește într-un nucleu al unui element. Atunci când un atom este neutru, înseamnă că el are același număr de protoni și electroni. Numărul atomic este notat cu un Z. Deoarece fiecare element are un număr diferit de protoni, acest număr este, de asemenea, utilizat pentru a reprezenta un element. Izotopii au de obicei acelasi numar atomic, dar sunt clasificati folosind masa lor atomica, de exemplu Carbon-12, Carbon-13.
Elementele sunt plasate în ordinea numărului atomic pe o masă periodică. Numărul atomic este afișat în colțul din stânga sus al elementului ca un superscript. Numerele atomice pot ajuta la divulgarea informațiilor despre element și mulți oameni pot vedea numărul atomic și să precizeze ce element este. De asemenea, acesta arată unde se poate plasa în tabelul periodic și dacă este lichid, gazos sau solid. Numărul atomic oferă, de asemenea, informații privind încărcarea nucleului, stările de oxidare, comportamentul de legare, încărcarea ionului etc.