Diferența cheie: Difuzia este procesul prin care moleculele se mișcă și călătoresc de la un loc la altul fără a necesita mișcare în vrac. Efuzia este procesul prin care moleculele călătoresc printr-o gaură de orificiu dintr-un loc de concentrație înaltă până la o concentrație scăzută.
Termenii difuzie și efuziune sunt frecvent utilizați în multe științe, cum ar fi chimia, fizica și biologia. În chimie, acești doi termeni sunt două proprietăți ale gazelor. Acestea două sunt confuze pentru mulți oameni care sunt doar de învățare de bază de gaze și proprietățile sale. Diffusion și Efusion sunt doi termeni diferiți care înseamnă două lucruri diferite și nu ar trebui să fie folosiți în mod interschimbabil. Difuzia se referă la capacitatea gazelor de a se amesteca unul cu celălalt, în timp ce efuziunea se referă la capacitatea gazului de a se deplasa printr-o gaură mică. Difuzia este folosită, de asemenea, în sociologie, economie și finanțe pentru a se referi la difuzarea oamenilor, a ideilor și a valorilor.
Difuzia este procesul prin care moleculele se mișcă și călătoresc de la un loc la altul fără a necesita mișcare în vrac. Difuzia rezultă în mișcarea sau amestecarea moleculelor numai prin utilizarea energiei cinetice. Cuvântul "difuzie" derivă din cuvântul latin "diffundere", care înseamnă "răspândirea". În difuzie, moleculele sunt într-o stare constantă de mișcare și atunci când sunt propulsate de energia cinetică sau termică, ele tind să se amestece cu alte molecule, rezultând un amestec inseparabil. Să luăm o abordare practică, un container este împărțit în secțiunile A & B folosind o partiție solidă; prima secțiune este umplută cu apă, în timp ce a doua secțiune este umplută cu vopsea roșie. Acum, când partiția este ridicată, vopseaua și apa încearcă să umple întregul recipient. Apoi colorantul încet încet roșiața de apă, aceasta fiind difuzia.
Difuzia determină trecerea moleculelor de la o zonă de concentrare mai mare la o zonă de concentrare mai mică, rezultând amestecul tuturor moleculelor. Difuzia se oprește atunci când toate moleculele sunt distribuite uniform. Difuzia nu se limitează la apă și funcționează cel mai bine în stări gazoase, unde moleculele au mai multă energie și capacitatea de a se amesteca cu alte molecule. Există două abordări ale difuziei: fenomenologice și atomice. Conform abordării fenomenologice, moleculele se deplasează din regiunile cu o concentrație mai mare în regiunile cu o concentrație mai scăzută. În abordarea atomică, difuzia este considerată a se întâmplă din cauza umblării aleatorii a particulelor difuzate, în care difuzia este propulsată de energia termică, determinându-le să se amestece împreună. Difuzia joacă un rol important în crearea mineralelor, nutrienților și energiei necesare corpului.

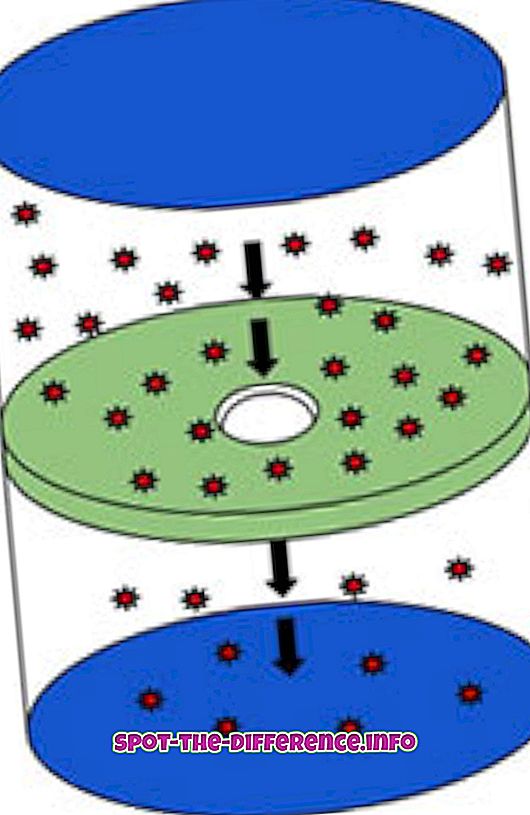
Efuzia este procesul prin care moleculele călătoresc printr-o gaură de orificiu dintr-un loc de concentrație înaltă până la o concentrație scăzută. Procesul descrie capacitatea gazului de a călători printr-o mică gaură fără coliziuni între molecule. Aceasta se întâmplă atunci când diametrul găurii este considerabil mai mic decât calea medie liberă a moleculelor. Calea liberă medie este distanța medie parcursă de o particulă în mișcare între coliziuni succesive. Un exemplu practic al acestui lucru ar fi umplerea unui container cu o sticlă cu fum și înghițirea unei găuri mici în flacon, fumul care începe să curgă din gaură este considerat ca efuzie.
Potrivit chimistului scoțian, Thomas Graham, care a creat formula pentru măsurarea efuzelor, a creat o lege Graham care determină cât de rapid va călători gazul și cum poate fi măsurat. Conform legii lui Graham, rata la care efuzul de gaze depinde de greutatea lor moleculară. Gazul cu o greutate moleculară mai scăzută va răsca mai repede decât un gaz cu o greutate moleculară mai mare. Efuzia se calculează prin măsurarea câtor molecule trece prin gaură într-o secundă. În mod similar, în termodinamică rata de efuzie a gazului este invers proporțională cu rădăcina pătrată a masei particulelor sale.