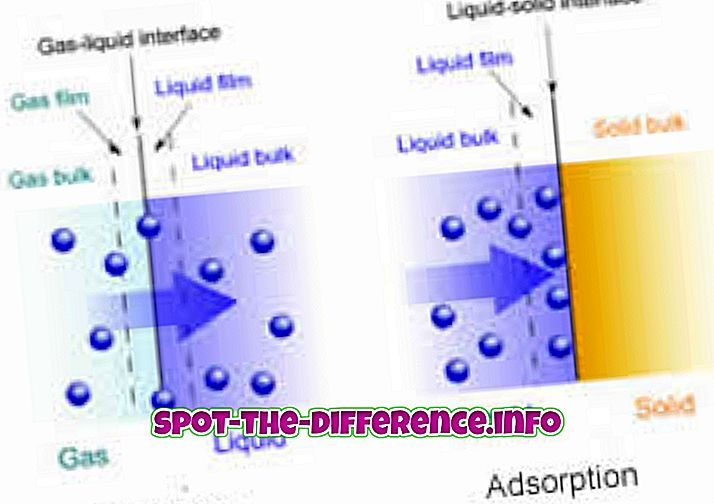
Diferența cheie: Absorbția este un fenomen în vrac în care un absorbant pătrunde complet în corpul unui solid sau lichid pentru a forma un compus sau o soluție. Pe de altă parte, adsorbția este un fenomen de suprafață în care moleculele unui adsorbat se concentrează numai pe suprafața unui adsorbant.
Reacția chimică - dioxidul de carbon absorbit de o soluție de carbon de potasiu
Procesul fizic - Aerul absorbit în apă prin dizolvare

Există două tipuri de moduri de adsorbție - chimice și fizice. În adsorbția chimică, moleculele și suprafața sunt legate de forțele slabe ale Vander Walls. Pe de altă parte, în adsorbția chimică, se formează o legătură chimică între molecule și suprafață.
Prin urmare, diferența principală dintre adsorbție și absorbție este că absorbția este un fenomen în vrac, ceea ce înseamnă că se întâmplă în întregul corp al materialului, în timp ce adsorbția rămâne un fenomen de suprafață. Adsorbția este întotdeauna exotermă, în timp ce absorbția este endotermă. Sorpția include atât procesele de absorbție, cât și adsorbția.
Comparație între adsorbție și absorbție:
Adsorbţie | Absorbţie | |
defintion | Acumularea unui gaz sau lichid dizolvat pe suprafața unui solid sau lichid | Difuzia unei substanțe într-un lichid sau solid pentru a forma o soluție sau un compus |
Exemplu | Gazele inerte sunt adsorbite pe cărbune. | Un burete uscat absoarbe apa |
Schimb de caldura | Exotermă, cu excepția adsorbției H2 pe sticlă | Endotermic |
Atingerea echilibrului | Comparativ mai rapid | Comparativ lent |
Concentraţie | Concentrația pe suprafața adsorbantului este diferită față de cea în vrac | Concentrația rămâne aceeași în întregul material |
Rata de apariție | Este rapid inițial, dar mai târziu rata începe să scadă | Ea are loc la o rată uniformă |